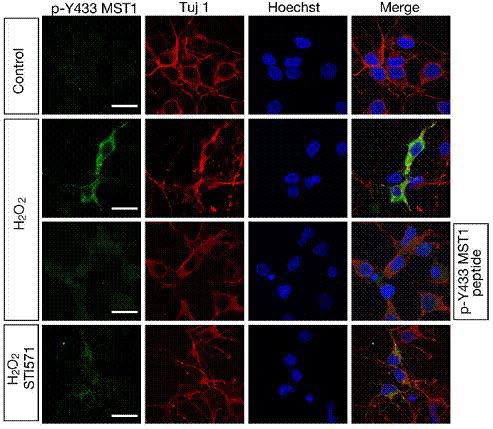
氧化应激影响细胞存活和体内平衡,但氧化应激的生物学效应背后的机制仍有待阐明。蛋白激酶MST1(哺乳动物Ste20样激酶1)在原代哺乳动物神经元中的氧化应激诱导的细胞死亡中起主要作用。然而,在氧化应激反应中调节MST1的机制仍然很大程度上未知。在本研究中,我们证明蛋白激酶c-Abl在Y433磷酸化MST1,其触发MST1的稳定和活化。 c-Abl的抑制促进HST70相互作用蛋白(CHIP)介导的泛素化的MST1至C末端的降解,从而减弱细胞死亡。氧化应激诱导MST1的c-Abl依赖性酪氨酸磷酸化并增加MST1和FOXO3(Forkhead box O3)之间的相互作用,从而激活MST1-FOXO信号传导途径,导致原代培养神经元和大鼠海马神经元中的细胞死亡。鉴定c-Abl酪氨酸激酶作为MST1的新型上游激活剂表明c-Abl-MST1信号级联在细胞对氧化应激的反应中起重要作用。